Гідракарбанаты

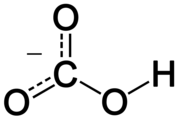
Гідракарбанаты — кіслыя солі вугальнай кіслаты H2CO3. Формула аніёна: HCO3-.
Гідракарбанаты шчолачных металаў растваральныя ў вадзе. Таксама добра растваральнымі ў вадзе гідракарбанаты шчолачназямельных металаў, уадрозненні ад карбанатаў.
Атрыманне
- Гідракарбанаты ўтвараюцца пры працяглым прапусканні CO2 праз раствор, які ўтрымоўвае карбанат:
C a C
O
3
H
2
O + C
O
2
→ C a ( H C
O
3
)
2
{\displaystyle {\mathsf {CaCO_{3}+H_{2}O+CO_{2}\rightarrow Ca(HCO_{3})_{2}}}}
- А харчовую соду атрымоўваюць па так званым аміячна-хларыдным спосабе:
N a C l + N
H
3
C
O
2
→ N a H C
O
3
N
H
4
C l
{\displaystyle {\mathsf {NaCl+NH_{3}+CO_{2}\rightarrow NaHCO_{3}+NH_{4}Cl}}}

Хімічныя ўласцівасці
- Пры награванні гідракарбанаты раскладаюцца на карбонат, ваду і вуглякіслы газ:
2 N a H C
O
3
→ N
a
2
C
O
3
H
2
O + C
O
2
{\displaystyle {\mathsf {2NaHCO_{3}\rightarrow Na_{2}CO_{3}+H_{2}O+CO_{2}}}}
- Гідроліз гідракарбанат-іона адбываецца па схеме:
H C
O
3
−
H
2
O ⇄ O
H
−
H
2
C
O
3
{\displaystyle {\mathsf {HCO_{3}^{-}+H_{2}O\rightleftarrows OH^{-}+H_{2}CO_{3}}}}

- Рэагуе з шчолачамі:
H C
O
3
−
O
H
−
→ C
O
3
2 −
H
2
O
{\displaystyle {\mathsf {HCO_{3}^{-}+OH^{-}\rightarrow CO_{3}^{2-}+H_{2}O}}}
- З кіслотамі:
H C
O
3
−
H
→
H
2
O + C
O
2
↑
{\displaystyle {\mathsf {HCO_{3}^{-}+H^{+}\rightarrow H_{2}O+CO_{2}\uparrow }}}
 Гл. таксама
Гл. таксама
Тэмы гэтай старонкі (1):Катэгорыя·Карбанаты


